HER2阳性乳腺癌的生物标志物
随着乳腺癌精准治疗时代的到来,乳腺癌的个体化治疗在目前分子分型的基础上不断突破,已经成为当下热门话题与追求目标。在精准治疗的目标下,需要针对肿瘤更精准的基因特征及危险因素,打造最优化的治疗方案。
2022年8月5日-7日 第五届肿瘤精准诊疗高峰论坛暨第八届乳腺癌个体化治疗大会(COMB)在北京隆重举行。诸多国内外乳腺癌专家重磅莅临,齐聚一堂,带来精彩的学术报告,并且在临床诊疗、当下科研热点以及未来发展方向方面充分交流意见。其中来自美国西北大学Robert H.Lurie综合癌症中心的肿瘤科主任William J. Gradishar教授,分享了目前HER2阳性乳腺癌精准治疗的研究进展,为HER2阳性乳腺癌个体化治疗之路带来了全新的思考。

1、基因检测技术发展助力精准治疗的广泛应用
William J. Gradishar教授指出,随着基因检测技术的发展,我们认识到乳腺癌的发生和发展受多个基因的多条信号通路调控,约80%的乳腺癌患者都存在基因突变。
目前,作用于不同通路/基因的靶向治疗药物如雨后春笋般出现,例如靶向HER2药物包括曲妥珠单抗、帕妥珠单抗、马吉妥昔单抗、T-DM1、T-DXd等。抗癌管家-康爱管家,我们一起抗癌,治愈癌症不是梦。还有小分子TKI药物,可在细胞内作用于HER2通路,包括拉帕替尼、图卡替尼、吡咯替尼等,针对不同信号通路,有不同的药物选择。由此,乳腺癌治疗的模式也从传统分型驱动转变为基因/分子分型驱动。
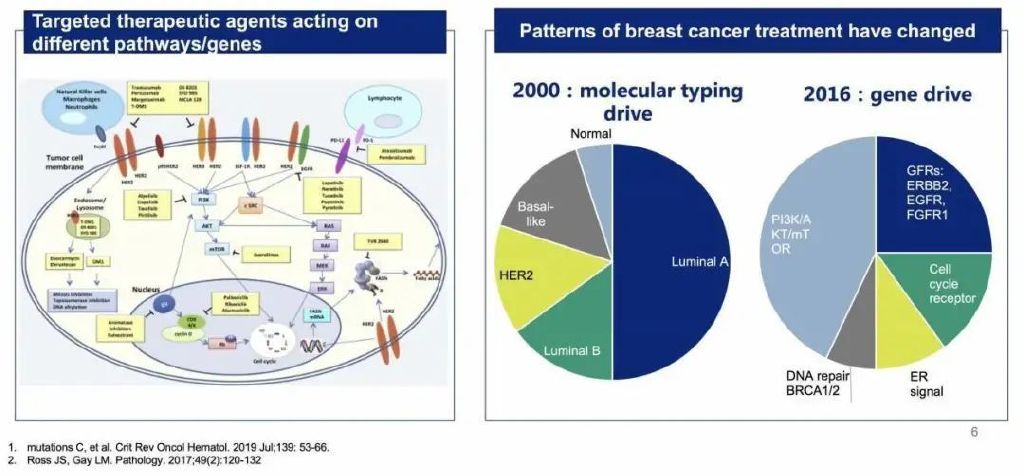
William J. Gradishar教授认为,肿瘤细胞与宿主免疫细胞的特征,是影响抗HER2治疗效果的重要因素。其中,肿瘤细胞的特征包括胞外受体蛋白表达情况:HER3/EGFR、HR和HER2共表达,及PD-L1;而肿瘤细胞内通路的信号异常,如PI3K/AKT/mTOR通路也需要特别关注。宿主免疫细胞的特征,主要是肿瘤浸润淋巴细胞 (TILs)和NK细胞的FcγRIIIA基因多态性。
2、HER2阳性乳腺癌的精准治疗策略升级
细胞外受体:HER3/EGFR、HR和HER2共表达、PD-L1
HER3至少在50–70%的乳腺癌患者中表达。CLEOPATRA研究和EMILIA试验结果显示,EGFR和HER3 mRNA高表达的患者可能从双靶点或 T-DM1治疗中获益。
William J. Gradishar教授还指出,ER表达会影响抗HER2治疗的获益程度。诸多试验如NeoSphere试验结果表明,曲妥珠单抗+帕妥珠单抗的双重HER2靶向作用产生了较高的病理完全缓解率。ER阳性患者的病理完全缓解率总是低于ER阴性的患者。而同时表达ER和HER2的患者可能对内分泌治疗耐药。
细胞内通路:PI3K/AKT/mTOR通路
不同分子亚型的乳腺癌患者具有不同的药物响应特点,在ER+乳腺癌中,PIK3CA突变的发生率约为40%。HER2阳性乳腺癌群体也是如此。多项研究均显示PIK3CA突变患者的治疗,与使用拉帕替尼相比,T-DM1的疗效更优。
肿瘤浸润淋巴细胞 (TILs) 和FcγRIIIA基因多态性
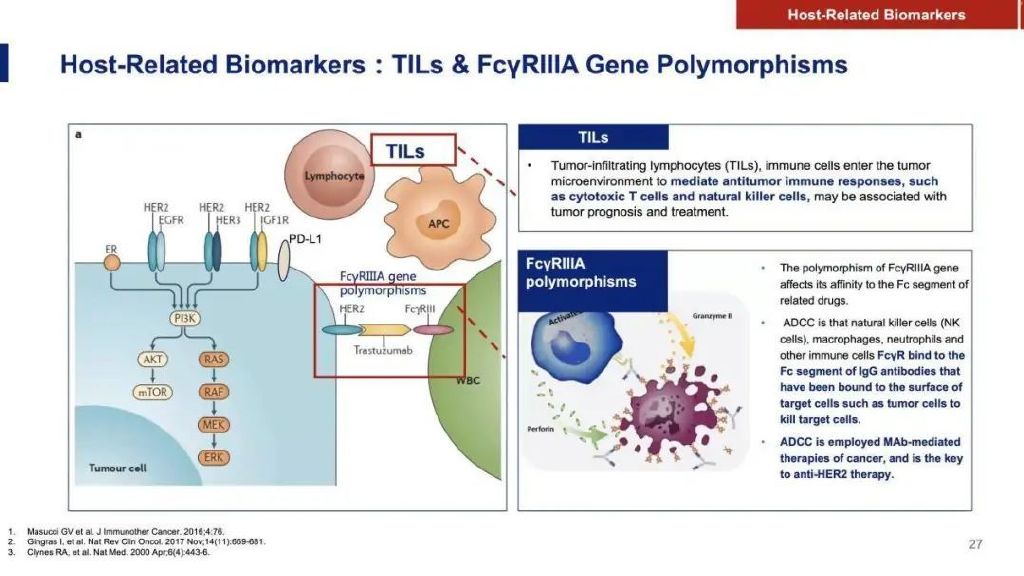
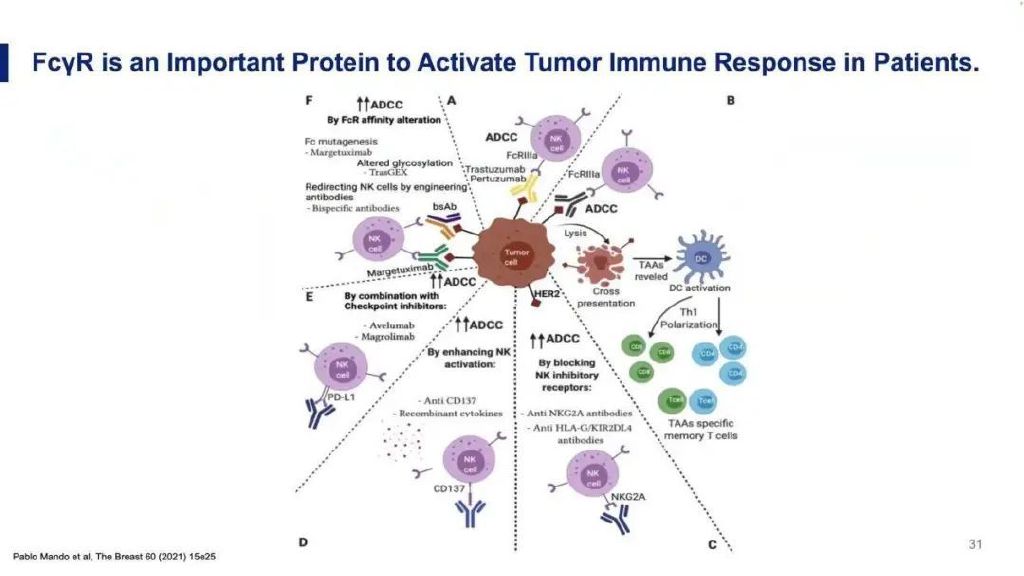
Fc受体能够与不同抗体相互作用,比如治疗性抗体、重组的细胞因子,或是记忆细胞等,对于免疫系统与药物治疗产生的细胞毒性之间的相互作用具有重要意义。Fcγ受体具有多态性,如V/V、V/F或F/F基因型。各基因型之间的表达存在差异。
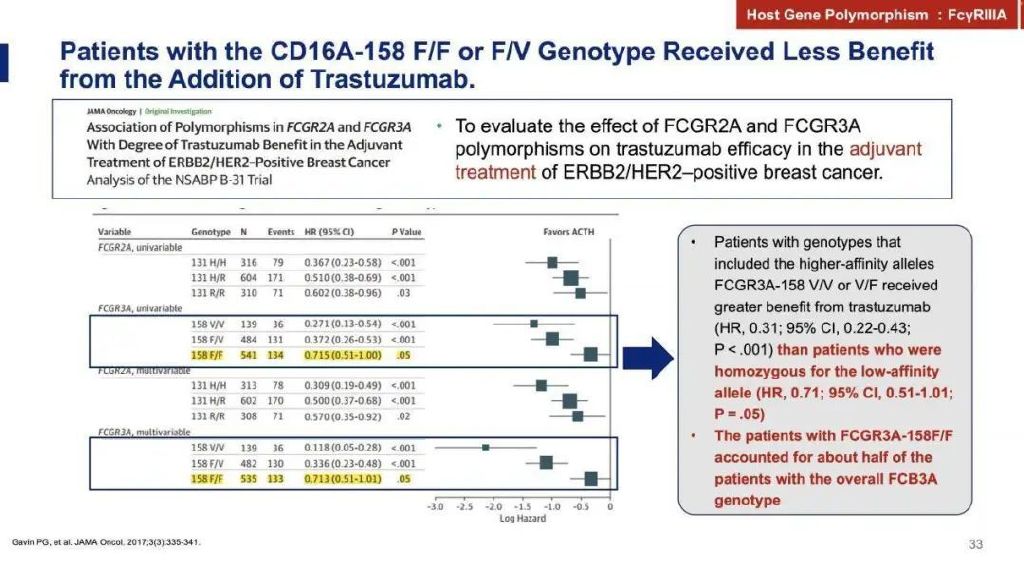
William J. Gradishar教授指出,FcγRIIIA受体可影响曲妥珠单抗在HER2阳性乳腺癌中的疗效,研究表明,对于CD16A-158 F/F或F/V基因型患者加用曲妥珠单抗的获益较少,患者治疗效果不佳,因此需要针对该亚型设计更有效的药物。
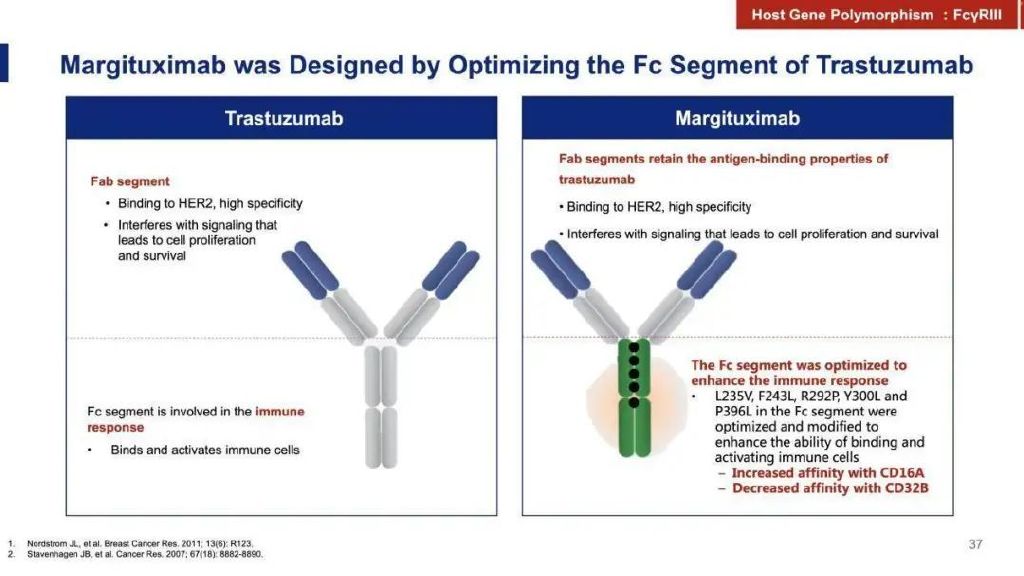
马吉妥昔单抗的问世为此类患者提供了全新的选择。相比于曲妥珠单抗,马吉妥昔单抗保留了能够与肿瘤细胞靶点(HER2)相互作用的Fab区域,其Fc部分经过工程化改造,使其对CD16A的亲和力增加,对CD32B的亲和力下降,通过增强免疫效能的方式整体提高对肿瘤细胞的杀伤作用。
上一篇:济企研发基因编辑技术“出口”美国
下一篇:瑞普生物2022年半年度董事会经营评述