《治疗性单克隆抗体CMC指南阅读笔记》
细胞系的开发包括构建一个合适的表达载体,并将该载体转入一个已经充分表征的宿主细 胞系。然后分离单细胞克隆,通过越来越严格的标准进行分析,直到确定首选和备选的生产细胞 系。图 5.1 是开发一个支持 IND/IMPD 过程的单克隆抗体产品的生产细胞系的经典工艺流程图。图 5.1 中列出的各个工艺步骤旨在说明一个典型的细胞系开发周期。具体使用的稀释和克隆程序,每 个阶段筛选的克隆数以及在每个阶段进行的前位克隆的评估会因公司而异,并且经常会因产品而 异。不管工艺的确切细节如何,细胞系开发的关键目标都是开发程序所产生的生产细胞系具有合 理的表达水平、能够在生物反应器中良好生长、遗传稳定性以及具有高度的单克隆性。
细胞系的开发通常都是在隔离的组织培养室中进行,房间应当彻底清洁并且有记录显示不 存在其他的细胞或者 DNA。通过将其与其他实验室工作的严格隔离,可以最大程度上降低获得错 误产物的细胞系的可能性。尤其是当公司正在开发多种单克隆抗体产品时,因为这些产品在早期 的分析方法上,比如 SDS-PAGE、SEC-HPLC 或者 CEX-HPLC 中不能有效区分(有关这些分析方法的 解释可参考第四章)。下面将会介绍生产细胞系开发的每个阶段的工作。
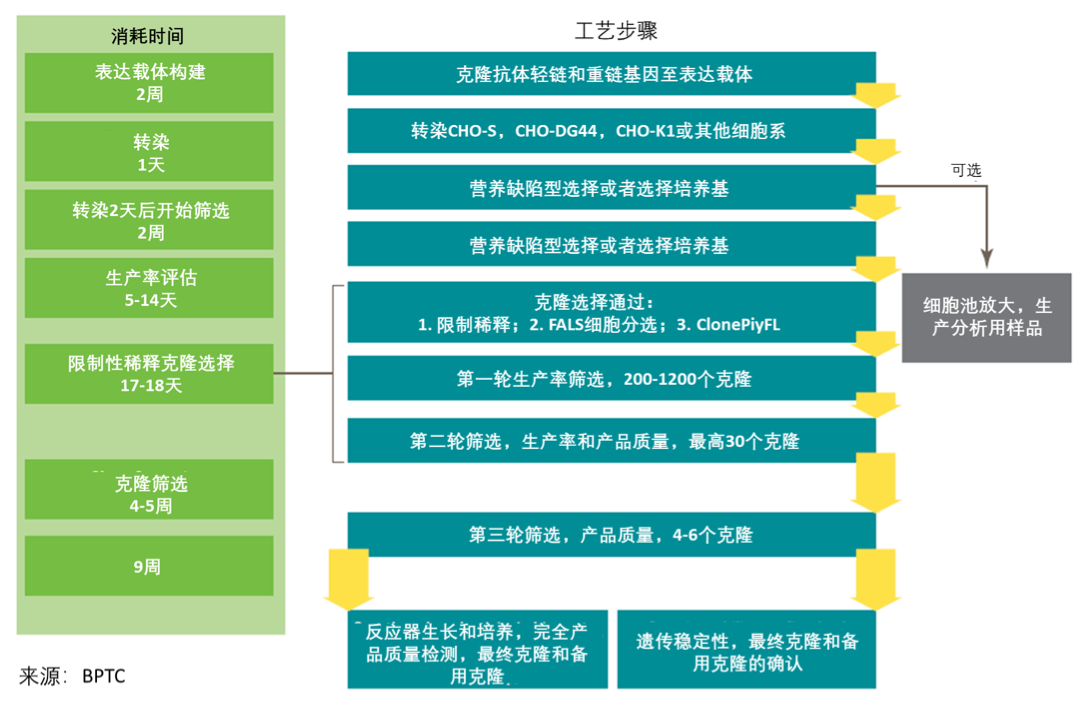
图 5.1 代表性的细胞株开发流程图。上图显示的是开发支持单克隆抗体产品 IND/IMPD 生产 型细胞株的代表性流程。是一个典型的细胞株开发生命周期。
表达载体的构建细胞系的开发工艺开始于表达载体的构建,该表达载体可以将编码单克隆抗体重链和轻链 的基因转入亲本细胞系。如表 5.3 所示,若要构建表达载体,需要设计、合成编码预期抗体重链 和轻链的基因,然后将其插入质粒载体中。
表 5.3 表达载体构建
活动 注意事项设计密码子优化的基因序列 外包给专业的服务商 (GeneArt,DNA2.0 或其他)
合成基因,限制酶切稳点适合 所用表达载体 外包,基因通常以临时载体形 式提供
克隆抗体基因至 1-2 个质粒载 体 构建完最终载体后进行基因序 列确认
哺乳动物细胞表达载体包括选择标记(比如 DHFR、抗生素抗性等)、转录调节元件(启 动子、增强子)、翻译起始序列、翻译增强序列和聚腺苷酸化信号序列。在大多数的表达载体中, 选择标记一般被有意的克隆到弱启动子的下游,而抗体基因被克隆至强启动子的下游。表达载体 可包含单或者双顺反子表达盒 ,两种方法都有合理之处。表达载体也可以包含其他功能的元件, 有助于表达载体的遗传稳定性,改善转录或者翻译速率亦或者改善整体的质粒生产效率。其中的 某些元件可能是有专利的,在这种情况下,必须获得技术所有者的授权才可以使用它们。专利系 统有助于更快速的鉴别具有高产品生产效率或者其他卓越性能特征的生产细胞系,但是应权衡 其优势和获得该技术所需的许可费或者特权使用费成本。
作为开发用于表达单克隆抗体产品的生产细胞系的第一步,还要尽量去优化重链和轻链基 因 DNA 序列翻译使用的密码子,以提高在宿主细胞中的有效翻译。尽量减少产物 mRNA 中可能阻 碍翻译过程的二级结构的形成。密码子的优化服务通常外包给少数的几个供应商,这些供应商提 供独特的密码子设计和优化程序作为其 DNA 合成服务的一部分。由于密码子的使用通常会极大的 影响抗体的翻译速率,因此在选择用于细胞系开发的基因序列之前,评估多个编码同一抗体的多 个 DNA 序列可能会有用的。翻译过程的错配、翻译后的加工和分泌都会导致重大的产品质量问题, 比如错配折叠或者聚集体,这将会严重影响下游工艺的开发。
一旦选择了特定的 DNA 序列并构建了表达载体,就需要对插入表达载体的重链和轻链基因 进行完整的测序,以确认在构建表达载体的所需操作中没有引入基因序列的错误。所有的监管机 构都希望对插入表达载体的基因进行测序,作为初始 IND/IMPD 提交的一部分。此外,较好的做法 还包括确认能够生产正确蛋白质的生产细胞系的开发时间和费用。无法确认表达载体中基因序列 将会导致单克隆抗体产品开发程序的延误或者失败。
转染在表达载体构建和序列测序完成之后,一般会通过转染将表达载体转入亲本细胞系,然后 进行培养,直到获得对数生长期的足够数量的活细胞,然后表达载体即被转入了细胞中。大多数 情况下,电转是常用的转染方法,因为该方法不会使亲本 CHO 细胞接触任何新的或者不完全鉴定 的试剂。其他的转染方法包括阳离子脂质体试剂 、聚乙烯亚胺(PEI)或者磷酸钙的方法,但 是这些方法不会用于转染用于 GMP 生产的细胞系。
上一篇:Beacon 单细胞光导系统
下一篇:央行降息後 廣州樓市一手二手齊打推盤攬客戰