T免疫细胞疗法行业深度报告:因病制宜,抗癌战
炒股就看金麒麟分析师研报,权威,专业,及时,全面,助您挖掘潜力主题机会!
1、 免疫细胞疗法:抗癌战场的尖兵锐器
细胞治疗是指通过生物工程技术,利用患者自体或异体某些具有特定功能的细胞 特性,经体外扩增、特殊培养处理后,使这些细胞具有增强免疫、杀死病原体和 肿瘤细胞的功能,从而达到治疗疾病的目的。
根据使用细胞标的的不同,细胞治疗分为:免疫细胞治疗和干细胞治疗。
免疫细胞疗法:采集人体自身免疫细胞如 T 细胞、NK 细胞、B 细胞和 DC 细胞等,经过体外改造、培养,使其数量扩增成千倍或增加其靶向杀伤能 力,然后再回输到患者体内,打破免疫耐受的同时,激活增强机体免疫力, 达到杀灭血液及组织中病原体、肿瘤细胞的目的。
干细胞疗法:将健康的干细胞移植到患者体内,修复、替换受损细胞及组 织从而治愈疾病。临床上常使用的干细胞种类有:间充质干细胞、造血干 细胞、神经干细胞以及皮肤干细胞等。
2012 年 1 月原卫生部叫停了中国大陆境内所有的干细胞治疗研究,2004~2012 年间药监局受理的 10 项干细胞新药注册申请被全部清零,使干细胞药物开发回 到原点。直至 2018 年 6 月,国家药监局才开始重新受理有关干细胞疗法的临床 注册申请,重启干细胞治疗在临床上的应用。因此截至 2022 年 3 月,我国还未 有一款干细胞治疗药品获批上市,市场较不成熟,投资价值有限,故本报告重点 对细胞治疗中免疫细胞疗法进行探讨。
广义的肿瘤免疫治疗可被分为非特异性和肿瘤抗原特异性两大类。其中,非特异 性肿瘤治疗主要是非特异性免疫刺激和免疫检验点阻断;而特异性肿瘤治疗则包 括肿瘤疫苗和免疫细胞疗法。这四类疗法的机理及特点如下:
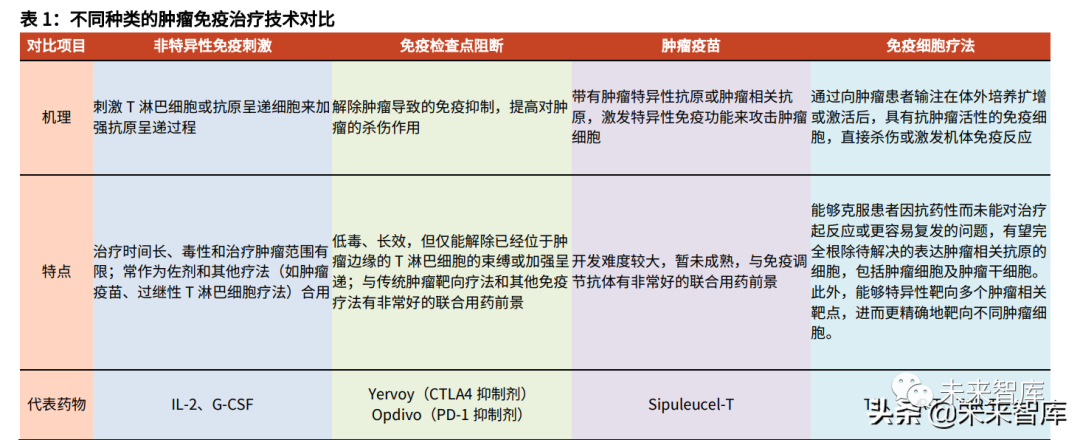
免疫细胞疗法最早可追溯至 1976 年科学家 Morgan 利用白介素-2(IL-2)诱导 LAK(Lymphokine Activated Killer)细胞治疗黑色素瘤、肺癌等多种恶性肿瘤。之后,历经 TIL、CIK 等疗法,最终迎来了新一代 CAR 以及 TCR 技术,临床显 示二者在抗肿瘤领域具有卓越的治疗效果。随 2017 年 8 月 FDA 批准诺华用于 治疗急性淋巴细胞白血病的 Kymriah 上市,免疫细胞疗法正式进入高速发展阶 段。
目前,国内外研究热度高且已取得重大进展的免疫细胞疗法主要分为 4 类:TIL (肿瘤浸润淋巴细胞,Tumorinfiltratinglymphocytes)疗法、CAR-T(嵌合抗 原受体,Chimeric Antigen Receptor)疗法、CAR-NK 疗法以及 TCR(工程 T 细胞受体,T-cell receptor)疗法。
1.1、 CAR-T 细胞疗法:血液瘤领域治疗优势凸显
1.1.1、结构及机理
CAR-T 细胞的结构主要包括:①抗原受体结构(single-chainvariable fragment, ScFv);②Spacer 结构域(或 Hinge 结构域);③跨膜结构域(Transmembrane Domain);④共刺激分子序列(细胞内信号序列,ITAMs)。
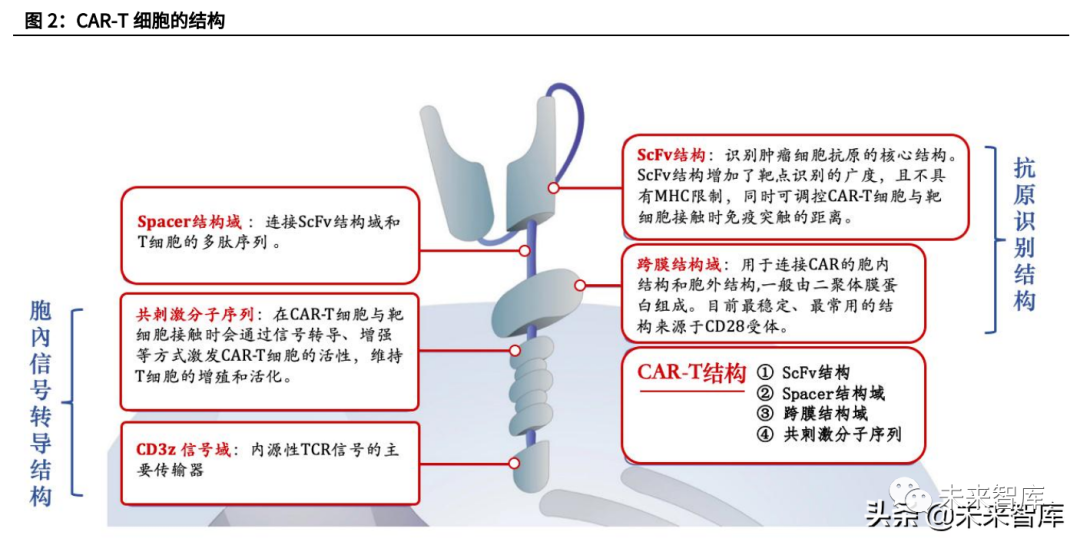
正常 T 细胞在行使杀伤作用前会与靶细胞结合,并在结合区形成免疫突触。同 样地,CAR-T 细胞也会靶向肿瘤细胞,并与靶细胞形成类似的免疫突触并启动免 疫反应。其主要通过以下三种机制杀伤肿瘤细胞:
① CAR-T 细胞分泌穿孔素和颗粒酶,穿孔素可以在肿瘤细胞表面“打洞”,随 后颗粒酶被输送至肿瘤细胞内部,通过物理作用直接杀伤肿瘤细胞或诱导肿 瘤细胞发生凋亡;
② CAR-T 细胞表面会高表达 TNF(肿瘤坏死因子)配体,这些配体可以诱导肿 瘤细胞凋亡;
③ CAR-T 细胞会分泌特定的细胞因子,这些细胞因子可以加强 CAR-T 细胞的 活性,进而改变肿瘤微环境,增强抗肿瘤活性。
1.1.2、结构优化历程
从 2002 年起,许多科学家致力于修饰、改造 CAR-T 结构的胞内信号转导区,以 进一步提高治疗效果。根据“共刺激分子序列”结构的不同,CAR-T 细胞可分以 下五代:
① 第一代:只有一个胞内信号组分(CD3ζ或 FcR·γ),T 细胞可被活化但无法 增殖,疗效甚微。
② 第二代:添加了共刺激结构域 CD28(代表产品:Yescarta)或 4-1BB(代 表产品:Kymriah)。含有 CD28-CD3ζ 结构域的 CAR-T 细胞:展现出更快更强的信号转导,可迅速分 化为效应 T 细胞;含有 4-1BB-CD3ζ 结构域的 CAR-T 细胞:可分化出在体内持续时间更长的记忆 T 细胞。
③ 第三代:含有两个共刺激结构域、三个胞内信号组分(CD3ζ、CD28、4-1BB 或 OX40)。三代 CAR 结构使细胞具有更强的肿瘤抑制、裂解能力。
④ 第四代:添加了自杀基因,可在具有免疫抑制性的肿瘤微环境中释放促炎性 因子,从而招募并活化更多的免疫细胞、增强免疫反应。
⑤ 第五代:通用型 CAR-T 细胞,突破个体限制,实现规模化生产和治疗。包括:通用 CAR 设计和通用 T 细胞设计。
上一篇:泰格医药:公司有开展大分子生物医药类业务临
下一篇:干细胞和免疫细胞的区别?