新药速递之Amivantamab (JNJ

【前言】EGFR 20插入突变患者约占EGFR突变的4%-12%,对于EGFR-TKIs 治疗效果不佳。2020年3月,美国FDA已授予美国强生公司新药Amivantamab(JNJ-61186372)突破性疗法认定,用于治疗接受铂类化疗期间或之后疾病进展的携带EGFR外显子20插入突变的转移性非小细胞肺癌(NSCLC)患者。在2020年ASCO会议上研究者进一步公布了JNJ-6372治疗EGFR 外显子20插入NSCLC患者的I期研究CHRYSALIS的初步结果,下面我们进一步了解一下JNJ-6372这个药物。
【药理作用】 JNJ-6372是一种EGFR-cMet双特异性抗体,通过与肿瘤细胞表面EGFR、c-Met受体结合阻断EGFR、c-Met信号通路激活,并具有降解肿瘤细胞表面EGFR、c-Met受体的作用及较强的抗体依赖性细胞毒作用。

图1 JNJ-6372结构示意图
【临床研究】

展开全文
图2 CHRYSALIS研究设计
CHRYSALIS研究是一项开放标签、多中心的I期临床研究,评估了JNJ-6372治疗晚期NSCLCL患者的安全性、药代动力学和疗效,
在2019年ASCO会议上,研究者公布了JNJ-6372的I期试验CHRYSALIS的初步结果。研究纳入了108例经治EGFR突变晚期NSCLC患者,32例患者达到PR,获益突变类型包括19del,L858R,G719A,T790M,20外显子插入的以及合并C797S或MET扩增的耐药突变患者。EGFR三代TKI耐药患者队列中,纳入58例患者,ORR 28%,在16例达到PR患者里包括了8例C797S突变,3例MET扩增,5例其它耐药机制(非EGFR耐药突变或MET扩增);EGFR EXON 20插入突变队列中,纳入27例患者,DCR 100%,8例PR患者达到PR,ORR 30%。

图3 2019年ASCO JNJ-6372整体人群获益情况

图4 2019年ASCO JNJ-6372在3代TKI耐药后人群获益情况

图5 2019年ASCO JNJ-6372在20插入人群获益情况
2020年ASCO会议上,研究者进一步公布了JNJ-6372的I期试验CHRYSALIS研究第二阶段 20 ins组(Cohort D)的初步结果。39例EGFR 20突变患者中ORR为36%,临床获益(达到PR及以上,或SD维持超过12月)的患者占67%,mPFS 8.3个月;对于既往接受含铂化疗的29例患者,41%患者病情缓解,临床获益率为72%,mPFS 8.6个月。
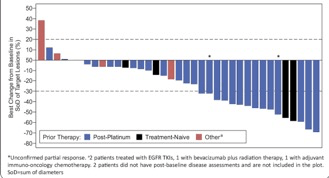
图6 2020年ASCO JNJ-6372在20插入(Cohort D)人群获益情况-1

图7 2020年ASCO JNJ-6372在20插入(Cohort D)人群获益情况-2
【用法用量】
根据CHRYSALIS 研究第一阶段剂量爬坡结果,目前第二阶段确定的单次用量为1050mg (<80kg)及1400mg(≥ 80kg)静脉输注,第一个周期1050mg或1040mg每周一次,第二个周期开始1050mg或1040mg每二周一次。
【安全性】
在第二阶段确定的用法用量的基础上,根据2020年ASCO报告,50例20ins患者接受JNJ-6372治疗,最常见不良事件是皮疹(72%),输液相关反应(60%)和甲沟炎(34%),输液相关反应一般出现在第一次输注,不影响后续治疗。其他与EGFR相关的不良事件包括口腔黏膜炎(16%),瘙痒(14%)和腹泻(6%)。36%的患者报告了3级及以上AE。其中没有3级以上皮疹,仅发生1例3级腹泻。3例(6%)的患者出现治疗相关≥3级AE,包括高淀粉酶血症、低钾血症、脂肪酶升高和肩/胸疼痛。3例(6%)的患者报告了与治疗相关的严重不良事件,如蜂窝织炎、间质性肺病、肩/胸疼痛。药物整体安全性可。
【问题】
(1)2019年ASCO报道的JNJ-6372治疗3代TKI耐药的队列,对于T790M伴797S突变患者的突变类型为顺式还是反式突变,尚未查阅到进一步说明,这方面有待Cohort C结果进一步的公布。
(2)CHRYSALIS研究排除了未经治疗的活动性脑转移患者,作为一个靶向EGFR的大分子抗体,其对血脑屏障的穿透性待进一步研究。前期基础试验提示JNJ-6372联合奥西替尼具有协同作用[1],目前一项Lazertinib联合JNJ-6372的临床研究正在开展中(NCT04077463),该研究允许纳入无症状未治疗的每个直径小于1cm脑转移患者。对于脑转移患者的单抗联合TKI的方式是否能取得一定疗效仍待后续研究结果公布。
【相关摘要】
2020 ASCO Abstract:9512 Amivantamab (JNJ-61186372), an anti-EGFR-MET bispecific antibody, in patients with EGFR exon 20 insertion (exon20ins)-mutated non-small cell lung cancer (NSCLC)
2019 ASCO Abstract:9009 JNJ-61186372 (JNJ-372), an EGFR-cMet bispecific antibody, in EGFR-driven advanced non-small cell lung cancer (NSCLC).
【参考文献】
[1]MLAS. L. Moores.等. "A Novel Bispecific Antibody Targeting EGFR and cMet Is Effective against EGFR Inhibitor-Resistant Lung Tumors." Cancer Research (2016).
上一篇:基于PiggyBac转座子系统构建随机突变体库的方法与
下一篇:788)正式纳入“突破性治疗药物品种”,将为中